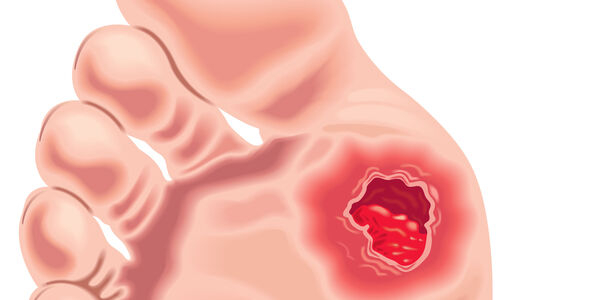
Das diabetische Fußsyndrom ist eine massive Folgeerkrankung des Diabetes. Rechtzeitiges Eingreifen, insbesondere präventive Maßnahmen, müssen im Vordergrund stehen. Wie das gelingen kann, erklärt Dr. Gerhard-W. Schmeisl in dieser Fortbildung.
In zwei Gerichtsurteilen des Sozialgerichtes Heilbronn (AZ S 12 KR 3527 /17 und S 12 KR 10 47/18) vom 16. Juli 2020 widerspricht dieses der Auffassung einiger medizinischer Dienste und Gutachter der Krankenkassen – und auch einigen Krankenhäusern – wonach ein "diabetisches Ulkus" nicht nur als Dekubitus (ICD-10-Code 289) kodiert werden darf sondern, dass neben der Wundtiefe auch eine Aussage über die Entstehung – nämlich einem Trauma/Druck von außen – und das Vorliegen einer Infektion oder nicht – berücksichtigt werden muss (posttraumatische Wundinfektion).
Die "Arbeitsgemeinschaft Diabetischer Fuß" (AG Fuß) hatte zu den Klagen der Diabetes Klinik Bad Mergentheim eine Stellungnahme verfasst: "Unzweifelhaft wird die Entstehung dieser Läsionen bei Menschen mit Diabetes als eine Kombination aus exogenen und endogenen Ursachen gesehen..." Eine durch die motorische Neuropathie und den Verlust der intrinsischen Fußmuskulatur entstehende Dysbalance mit Verlagerung knöcherner Fußanteile unter die Haut, bei gleichzeitiger Verlagerung und Minimierung von Polsterstrukturen machen den Fuß verletzlicher (endogen), es kommt zur Verlagerung von Fuß-Anteilen in belastete Zonen, die für diese Belastung nicht vorgesehen sind, und durch rezeptive (Micro-) Traumatisierung zu Überlastungserscheinungen (Schwielenbildung) und dann durch fortgesetzten Traumatismus (exogen) bei fehlendem warnendem Schmerzempfinden zu einem aktiven diabetischen Fußsyndrom mit zunächst oberflächennahen Folgen der Resistenzminderung, was im Verlauf zu einem Ulcus führt. Wenn dieses dann weiter belastet wird, kommt es zu einem fortgesetzten Traumatismus der "Wundregion" und häufig zu posttraumatischen Wundinfektionen.
Diese Stellungnahme der AG Fuß berücksichtigt, dass es ohne ein entsprechendes Trauma von außen bei den meisten Menschen mit Diabetes und Polyneuropathie nicht zu einer Fußläsion kommt.
Obwohl etwa bis zu 70% der Menschen mit Diabetes mit diabetischem Fußulcus eine Neuropathie haben, kommt es nur in etwa 30% zu einem akuten diabetischen Fußsyndrom. Dies erklärt sich durch das schon zuvor beschriebene und dann immer vorhandene Zusammentreffen von endogenen und exogenen Faktoren (https:ag-fuss-ddg.de/9/20). Die lebenslange Inzidenz von Ulcera bei Diabetes liegt bei etwa 25% – bei mehr als 50% der Betroffenen kommt es zu einer Infektion. Das Sterberisiko für einen Patienten mit diabetischem Fußsyndrom ist dabei innerhalb von fünf Jahren doppelt so hoch wie bei einem Patienten ohne Fußsyndrom! (Sigl, Amendt – Diabetes aktuell 7/2021).
Was macht denn nun ein diabetisches Ulcus so besonders?
Es handelt sich um eine Läsion unterhalb des Kniegelenkes:
- Eine initiale Läsion (z.B. ein Druckulcus, infizierte Wunde)
- Eine chronische Wunde, die länger als 8 Wochen ohne Heilungstendenz imponiert (trotz erfolgter Behandlung)
- Die "diabetische neuropathische Osteoarthropathie" (=Charcot-Fuß) mit den Zeichen:
- - Wärme
- - Schwellung
- - Rötung
- - Schmerz
- - Oder radiologischem Befund (mind. 2 klinische Zeichen müssen vorhanden sein
- Ein Zustand nach Amputation mit gefährdetem Stumpf oder mit besonderer Gefährdung nach abgeheiltem Ulcus. (s. Praxisbibliothek, Kirchheim Verlag 2018
Druckulcera weisen durch ihre Lokalisation auf die spezifische Störung der Biomechanik hin. Daraus lässt sich in vielen Fällen die richtige Art des Entlastungskonzeptes ableiten (Entitätenkonzept D. Hochlehnert et al.). Kommt es erst zu einer Wundinfektion, dann fehlen bei der diabetischen Polyneuropathie oft die üblichen Schutzfunktionen. Kommt darüber hinaus noch eine Durchblutungsstörung der Beine zum Tragen, im Sinne einer peripheren Angiopathie/periphere AVK, dann wird es gefährlich. Wenn jetzt nicht rechtzeitig sowohl lokal als auch bezüglich der Durchblutungsstörung, z.B. mittels Eröffnung mit einem Katheter (PTA) behandelt wird, steigt das Risiko einer Amputation deutlich an. Bagatellverletzungen sind häufig die Ursache, z.B. durch:
- Falsches oder zu enges Schuhwerk
- Falsche Druckbelastung
- Entzündungen, die nicht innerhalb weniger Tage oder Wochen abheilen
- Evtl. zusätzliche Pilzinfektionen im Bereich der Zehenzwischenräume und der Zehennägel.
Was macht die diabetische Wunde so besonders gefährlich?
1. Diabetische Polyneuropathie
2. Diabetische Angiopathie
a) Diabetische Mikroangiopathie
mit Stenosen und Verschlüssen von Endstromgefäßen, besonders an:
- Nierenglomeruli
- Netzhautgefäßen
b) Diabetische Makroangiopathie
an
- peripheren Arterien (pAVK)
- Herzkranzgefäßen (KHK)
- Hals-und Hirngefäße (Apoplektischer Insult)
Typisch für die Beschwerden der Polyneuropathie sind das Kälte-und Taubheitsgefühl, wobei es sich um eine subjektive Empfindung handelt, da sich die Zehen und Fußsohlen beim Anfassen meist warm anfühlen, Folge einer Neuropathie-bedingten Sympathikolyse. Neben diesen "sockenförmig" imponierenden Beschwerden kommt es später meist zu einer Störung des Berührungs- und Vibrationsempfindens, letztlich oft auch zu motorischen Schäden, die als Atrophie der kleinen Muskeln imponieren. Der zunehmende Verlust von Schweißdrüsen führt zu Hyperkeratosen und trockener, sehr empfindlicher Haut. Die Ursache der Neuropathie ist, sowohl vaskulärer Natur (Mikro - und Makroangiopathie), als auch metabolischen Ursprungs (Aldose Reduktase-Stoffwechsel) mit Zerstörung sympathischer Fasern (Auto - Sympathektomie). Eine irreparable Gefäßweitstellung und der Verlust der vaskulären Anpassung an variable Zirkulationsbedingungen sind die Folge. Die späteren Schädigungen des knöchernen Fußskelettes im Rahmen der diabetischen neuropathischen Osteoarthropathie beruhen ebenfalls auf den beschriebenen pathophysiologischen Veränderungen. Die klassische Mikroangiopathie des Diabetes ist eine komplexe Form der Zirkulationsstörung der Endstrombahn. Sie setzt sich aus vaskulären Veränderungen und einem rheologischen Faktor zusammen, rheologisch bedeutet eine erhöhte Viskosität von Blut-und Plasma (Hyperfibrinogenämie) und eine veränderte Verformbarkeit der Erythrozyten (Tabelle 1).
Man unterteilt die diabetische Angiopathie in eine Mikro-und eine Makroangiopathie, die beide meist gemeinsam vorkommen, jedoch unterschiedliche Bedeutung haben.
Die diabetische Makroangiopathie weist ein relativ typisches Verteilungsmuster auf. Neben der A. femoralis profunda sind vermehrt auch die infrapoplitealen Arterien betroffen (schlechte Kollateral-Versorgung). Der Diabetes mellitus gehört neben dem Rauchen, der Hyperlipoproteinämie und der arteriellen Hypertonie zu den größten Risikofaktoren der peripheren arteriellen Verschlusskrankheit (pAVK) – beide sind chronische fortschreitende Erkrankungen. Letztendlich ist die schlimmste Komplikation beider Erkrankungen die Oberschenkel- und Unterschenkelamputation (Major-Amputation).
Eine pAVK erhöht auch das Risiko einer Wundheilungsstörung und damit auch für eine Infektion und Amputation. Etwa 20% der mittelschweren und schweren diabetischen Fußinfektionen führen zu einer Amputation (Sigl M, Amendt K, Diabetes aktuell 7/2021).Die Möncheberg’sche Mediasklerose, eine oft röhrenförmige Sklerosierung der Tunica der Arterien, bedeutet per se keine Stenosierung oder Verschluss von Arterien.
Die periphere Mikroangiopathie ist ein komplexer Prozess. Viele Jahrzehnte hatte man die Vorstellung von diabetisch spezifischen Verschlüssen auf arterioler bzw. auf kapillärer Ebene. Eine neue Sicht hat dazu geführt, dass heute invasive Verfahren an Bedeutung gewonnen haben (PTA, Bypass). Veränderungen der Blutkomponenten mit Viskositätssteigerung und einer Hyperkoagulolabilität, die eine zusätzliche Störung der Mikrozirkulation verursachen, kommen hinzu. Nekrosen und auch eine Gangrän werden meist durch die "diabetische Makroangiopathie" verursacht.
Eine weiterführende Diagnostik klärt in der Regel den genauen Gefäßstatus mittels Pulspalpation, ABI-Messung und Duplex-Sonographie/Farbduplex-Sonographie. Ein Ancle-Brachial Index – mittels ABI-Messung (Dopplerdruck) ermittelt – unter 50mmHg gilt nach den Richtlinien als ein kritischer Wert für eine Ischämie und erklärt in der Regel das Vorhandensein einer Nekrose oder Gangrän!
Ergänzend wird die Bestimmung des transkutanen Sauerstoffpartialdruckes TCPO2 durchgeführt. Wenn die Infektion unter Kontrolle ist, der Patient bezüglich des Stoffwechsels stabilisiert ist, sollte bei schwerwiegender AVK eine weiterführende angiographische Diagnostik erfolgen. Die Läsion sollte nach dem Ausmaß der Gewebezerstörung und nach dem Vorliegen einer Infektion und/oder einer Ischämie beurteilt werden. Dazu hat sich die Wagner/Armstrong-Klassifikation sehr bewährt.(Tabelle 2)
Heute gilt insbesondere bei isolierten Unterschenkelverschlüssen als Mittel der Wahl ein Bypass bzw. auch eine perkutane transluminale Angioplastie (PTA), vor allem bei kurzstreckigen Verschlüssen besonders im Tibio-peronealen Übergang. Langstreckige infrapopliteale Verschlüsse werden in der Regel mittels Bypass-Chirurgie versorgt (z.B. "distal-origin Bypass-Chirurgie") und regelmäßig mittels Duplex-Sonographie kontrolliert.
Medikamentös gibt man in der Regel 100mg/Tag Acetylsalicylsäure (ASS) als Thrombozyten-Aggregationshemmer. In einigen Fällen auch das Clopidogrel (ADP-Rezeptor-Antagonist) insbesondere bei Unverträglichkeit des ASS. Bei komplexen Stenosen ist nach neueren Studien zusätzlich zum ASS auch eine niedrige Dosis eines Faktor Xa-Hemmers möglich (Rivaroxaban).
Was muss man unbedingt bei der praktischen Wundbehandlung berücksichtigen?!
Die Behandlung sollte durch ein interprofessionelles Team multiprofessionell und transsektoral durchgeführt werden. So ist nach der Berechnung der Kostenträger und verschiedener Gesellschaften eine Senkung der Amputationshäufigkeit um mehr als 50% möglich.
Neben der Stoffwechseloptimierung, der Therapie von Gefäßverschlüssen und der Behandlung evtl. vorhandener internistischer Grunderkrankungen, sowie der Infektionskontrolle steht praktisch im Vordergrund:
- Wunddebridement
- Druckentlastung
- Lokale Wundbehandlung
Wenn eine lokale Wunde nach etwa 8 Wochen trotz Therapie keine Heilungstendenz zeigt, muss unbedingt nach anderen differentialdiagnostischen Ursachen geforscht werden. In der Regel sind es Durchblutungsstörungen oder auch eine noch nicht adäquate Blutzuckereinstellung. Das Risiko der Übertragung von Infektionserregern aus einer chronischen Wunde, aber auch die Besiedlung der Wunde selbst mit Bakterien aus dem Patientenumfeld, geschieht meist durch die an der Pflege beteiligten Personen, insbesondere während des Verbandswechsels. Zur Verhinderung der Erregerübertragung und weiterer Wundinfektionen sind deshalb besondere Hygienemaßnahmen (AWMF, Arbeitskreis Krankenhaus und Praxishygiene) erforderlich. Neben der Händedesinfektion (vor und nach jedem Patientenkontakt, Einwirkzeit beachten) und dem Ablegen von Ringen, Uhren und Armbändern ist es das Tragen von kurzärmliger Kleidung, um eine Kontamination zu vermeiden. Bei entsprechendem Risiko ist auch das Tragen von Schürzen oder Schutzkitteln erforderlich. Ansonsten unsterile medizinische Schutzhandschuhe aus Gründen des Arbeitsschutzes und die Möglichkeit die notwendigen sterilen medizinischen Hilfsmittel wie Messer, Spatel, Scheren, Pinzetten auch steril ablegen zu können (Non-Touch-Technik).
Therapieprinzipien
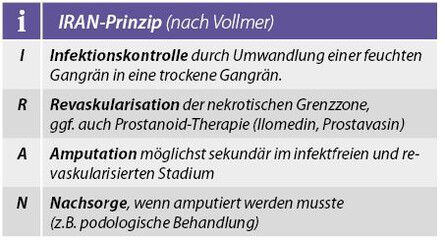
Bei Vorliegen einer diabetischen Mikro-, bzw. Makroangiopathie sollte man zunächst das IRAN-Prinzip nach Vollmer anwenden (rechts).
Vorgehen bei einem Verbandswechsel
Alle Materialien werden auf einem flächendesinfizierten Wagen o.ä. bereit gelegt (Einwirkzeit beachten!). Nach Händedesinfektion und dem Anziehen von Einmalhandschuhen wird der alte Verband entfernt. Die Handschuhe werden nun ausgezogen und entsorgt, die Hände erneut desinfiziert. Nach dem erneuten Anziehen von Handschuhen wird z.B. mit einer sterilen Pinzette und sterilen Kugeltupfern die Wunde je nach Größe mit sterilen Flüssigkeiten (z.B. Ringerlösung) – nicht mit Leitungswasser (dies könnte mit Pseudomonas kontaminiert sein!), ausgespült und mit z.B. Octenisept® oder Polyvidon® von außen nach innen desinfiziert.
Das anschließende Wunddebridement (Entfernung von Hornhaut und totem Gewebe!) erfordert meist die größte Arbeit. Nach der Entfernung von abgestorbenem Gewebe, sieht die Wunde oft schon ganz anders aus, außerdem sind nur so eventuelle Fistelgänge zu entdecken.
Erst nach erneuter Desinfektion wird die Wunde mit einem entsprechenden Wundverband bedeckt und sämtliches infizierte Material und "Werkzeug" sicher entsorgt.
Ein Verbandswechsel erfolgt anfangs meist täglich – manchmal auch 2x täglich – bei deutlicher Heilungstendenz auch alle 2-3 Tage. Ein Wunddebridement muss meist einmal wöchentlich erfolgen – besonders zur Entfernung der Hornhaut und verhärteter Wundränder ("anfrischen!")!
Wundverbände
Was versteht man unter einem idealen Wundverband? Er:
- führt zu einer Aufrechterhaltung eines feuchten Milieus im Wundbereich,
- dient dem Entfernen von überschüssigen Exsudat und toxischen Substanzen,
- führt zu einer thermischen Isolation der Wunde,
- ermöglicht einen Gasaustausch
- hinterlässt keine Fremdartikel oder toxische Stoffe
- schützt vor Sekundärinfektionen.
Merke: Der Verbandwechsel sollte atraumatisch sein, aber auch die Wirtschaftlichkeit sollte man im Auge behalten. Es sollten keine "veralteten Wundtherapeutika" eingesetzt werden:
- keine die Anwendung lokaler Antibiotika – obsolet und veraltet
- kein Refobacin®
- Keine Farbstoffe wie Mercurochrom®, Rivanol®, Kaliumpermanganat® oder Brilliantgrün®
- Die lokale Anwendung von Traubenzucker oder Zucker, Speisehonig, Zinkpaste oder Wasserstoffperoxid ("steriler Honig" in Auflage möglich!) ist ebenso veraltet/experimentell.
Als "Antiseptika" werden primär auf Grund eines Konsensus heute verwendet:
- Providon Jod (PVP-Jod),
- Octenidin Hydrochlorid (=Octenisept®) und
- Polyhexamed (= Polyhexanid® 0,4%/0,6%)
Bei akut infizierten bzw. kolonisierten Wunden sollten kurzzeitig PVP Jod oder Octinidin-basierte Antiseptika verwendet werden, bei chronischen schlecht heilenden Wunden ist Polyhexanid das Mittel der 1.Wahl, auch über einen längeren Zeitraum.
Hydrogele bieten insbesondere bei trockenen bis mäßig exsudierenden Wunden, aber auch bei nekrotisch belegten schmierigen Wunden viele Vorteile.
Alginate verwenden wir insbesondre bei tiefen, zerklüfteten Wunden mit Wundtaschen, stark nässenden bis stark sezernierenden und schmierig belegten Wunden. Gelegentlich werden auch silberhaltige Wundauflagen verwendet, insbesondere wegen der hohen antiseptischen Wirkung – dadurch und auch bei gleichzeitiger Verwendung von Kohle lässt sich gerade eine sehr stark riechende Wunde sehr erfolgreich behandeln.
Wunddistanzgitter z.B. aus Silikon oder auch spezielle PU-Folien können einem Verkleben der Wunde vorbeugen.
Man sollte die verschiedenen Wundauflagen sowohl in der Klinik als auch in der Praxis gezielt austesten und sich bei positivem Verlauf auf wenige bekannte Materialien beschränken. Das gesamte therapeutische Team sollte erprobte Materialien verwenden, um damit Erfahrungen zu sammeln.
Neue hilfreiche Verbände?!
Nachdem Jahrzehnte lang eine "trockene Wundbehandlung" durchgeführt wurde (Verwendung von trockenen Kompressen!), ist heute die feuchte Wundbehandlung aus pathophysiologischen Gründen Standard. Aktuell werden sogar noch "neuere" Auflagen getestet, die der Haut von Fruchtblasen oder dem Dünndarm von Rindern und Schweinen entstammen. Wenn diese von tierischen Zellen befreit sind, dienen sie als Basis (Matrix / Gerüst) dafür, dass sich menschliche Hautzellen einnisten können (R.Door 2018). So soll auch die Haut des nordatlantischen Dorschs (Dr.H.Diener, Uni Hamburg), die wohl der menschlichen Haut sehr ähnelt, zur Ansiedlung von menschlichen Stammzellen dienen. Positiv: Sie enthält wohl einen hohen Gehalt an Omega-3-Fettsäuren.
Madenlarven als biologisches Skalpell
Schon lange werden insbesondere bei stark sezernierenden und zerklüfteten Wunden Larven der Goldfliege, eingepackt in kleine Säckchen verwendet. Diese sind so gestaltet, dass die Insekten zwar "totes Gewebe" aus der Wunde aufnehmen, nachdem durch das Sekret der Larven dieses aufgelöst wurde, ihren Platz im Säckchen jedoch nicht verlassen können - sie fressen nur totes Material (Lucilia sericata). In den Anfängen der Therapie gab es zunächst auch "Freiläufer", dies wurde von den Patienten jedoch oft als "ekelig" empfunden.
Vakuumtherapie (VAC-Therapie)
Neuerdings kann diese sehr segensreiche Therapie auch auf Rezept zu Lasten der gesetzlichen Krankenkassen bei ambulanten Patienten verordnet werden. Bei der Vakuum Therapie wird eine Wunde mittels einer Folie Luftdicht versiegelt und über eine Pumpe laufend Sekret abgesaugt. Dies führt oft relativ schnell zu einer Säuberung der Wunde und auch zu einer besseren lokalen Durchblutung sowie zu einem Wachstumsreiz der Hautzellen.
Hyperbare Sauerstofftherapie
Bei dieser Therapie wird vom Patienten reiner Sauerstoff unter einem Druck von 2 bis 3 bar eingeatmet. Verschiedene Studien zeigen zwar angeblich eine Verbesserung der Sauerstoffversorgung der Wunde – der die DDG jedoch widerspricht – es gab jedoch besonders bei kardial vorerkrankten Menschen kritische/ tödliche Zwischenfälle. Die Kosten werden von den Leistungsträgern übernommen (aktueller Stand), sollte aber bei kardial vorerkrankten Menschen nicht durchgeführt werden.
Kaltes Plasma
Kaltes Plasma ist bei der Behandlung von komplexen Wunden als nicht - invasives Verfahren (zum Beispiel Plasmaderm) bekannt. "Plasma kann man sich als ein energiegeladenes leuchtendes Gas vorstellen (Dr. J Ernst, Göttingen)". Wird einem Gas weiter Energie zugeführt, geht es in den Energiereichen Plasmazustand über (4. Aggregatzustand).
Die therapeutischen Wirkungen scheinen durch 3 Wirkmechanismen zu entstehen:
- Stimulierendes elektrisches Feld
- UV- A-und UV- B-Licht
- Aktivierte Gas-Spezies-Ozon, Sauerstoff
Die Anwendung soll einfach und sehr effektiv sein (Plastische Chirurgie Uni Göttingen Dr. J.Ernst) – es kann auch ambulant durchgeführt werden (Fa.Cinogy, GmbH).
Per definitionem gilt aber eine Wunde, die nach 8 Wochen nicht abklingt als "chronisch" (ICW - Initiative chronische Wunden). "Eine chronische Wunde ist eine durch Zellschädigung, Zerstörung oder Trennung vom Körpergewebe bedingter pathologischer Zustand, oft verbunden mit einem Substanzverlust sowie einer Funktionseinschränkung (Protz, 2007).
Wo liegt der "wunde Punkt" bei chronischen Wunden?
Die Chance, dass eine Wunde abheilt und eventuell auch nicht wiederkommt, hängt davon ab, deren Genese und eventuell vorhandene Hemmnisse wie zum Beispiel Begleiterkrankungen rechtzeitig zu erkennen und gleichzeitig zu behandeln. So ist ein einheitliches zielgerichtetes Handeln nicht nur bezüglich der Wunde notwendig. Die Diagnostik und die Therapie sollten deshalb nach inzwischen von zahlreichen Fachgesellschaften und Initiativen aufgestellten Leitlinien beziehungsweise Behandlungspfaden durchgeführt werden.
Allerdings ist auch klar: Je mehr engagierte und interessierte Ärzte sowie Krankenschwestern, Pfleger, Podologen und Wundmanager an der Behandlung beteiligt sind, desto größer sind die Chancen des Betroffenen. Interprofessionelle und interdisziplinäre Kooperationspartner arbeiten in einer Art offener Netzwerk - Struktur zusammen Dies ist im positiven Falle gut für den Patienten und wirklich auch finanziell günstiger für unsere Gesellschaft (Wirtschaftlichkeit?!).
Wie erfolgt die Diagnose einer chronischen Wunde?
Die Diagnose einer chronischen Wunde ist die Basis einer erfolgreichen Behandlungsstrategie – diese sollte sich an den ABCDE -Regeln orientieren. Da Bakterien selten die alleinige Ursache chronischer Wunden sind, ist ein oberflächlich abgenommener bakteriologischer Abstrich für Screening -Untersuchungen z.B. MRSA sinnvoll – dabei sollte vorher keine Wundsäuberung durchgeführt werden (Essener Kreisel). Bei klinischem Verdacht auf eine Wundinfektion sollte dagegen vor einer bakteriologischen Diagnostik eine Wundsäuberung zum Beispiel mit physiologischer Kochsalz –bzw. Ringer- Lösung und sterilen Kompressen durchgeführt werden (Levine - Technik in dem klinisch infizierten Areal), Biopsien bei tieferen Ulzerationen z.B. dem diabetischen Fußulcus sind sinnvoll. (Tabelle 3)
Zur Frage, ob eine lokale Wunde antiseptisch behandelt werden sollte, hat sich der TILI-Score bewährt: Diese ist gegeben, wenn alle 6 Merkmale vorhanden sind:
- Periläsionales Erythem
- Überwärmung
- Ödem, Verhärtung, Schwellung oder Nekrose
- Spontanschmerz oder Druckschmerz
- Stagnation der Wundheilung Anstieg und oder Änderung der Farbe oder des Geruchs des Exsudats
Ausnahme: 4 Merkmale reichen aus, wenn folgendes vorliegt:
- Nachweis von MRSA
- Nachweis von P. aeruginosa und mindestens 2 lokale Infektionszeichen
- chirurgische septische Wunde
- freier Eiter

Zusammenfassung
Menschen mit einem Diabetes – evtl. noch kombiniert mit einer peripheren arteriellen Verschlusskrankheit, Fettstoffwechselstörungen und einem erhöhten Blutdruck, haben ein besonders hohes Risiko für eine Amputation, aber auch für andere Kardio-vaskuläre Komplikationen.
Die interdisziplinäre Behandlung einer Wunde bei diabetischem Fußsyndrom mit geteilter Verantwortung ("shared decision") von Spezialisten kann, wie Studien belegen, die Inzidenz von Major-Amputationen um 75% reduzieren (Holstein P et al Diabetologia 2000; 43: 844-847). Eine adäquate Wundversorgung ist auch während der jetzigen Corona-Pandemie nicht immer gewährleistet gewesen (Rogers LC et al. Am Podiatr Med Assoc 2020; 110).
Liebe Diabetes-Forum-Leser, liebe Mitglieder des Verbandes der Diabetes-Beratungs- und Schulungsberufe in Deutschland e. V. !
In regelmäßigen Abständen gibt es in unseren Diabetes-Forum-Ausgaben Fortbildungsbeiträge. Zusammengestellt sind die informativen Artikel von Dr. Gerhard-W. Schmeisl aus Bad Kissingen. Thema diesmal: "Diabetisches Fußsyndrom – Wundmanagement". Die Mitglieder des VDBD und auch alle anderen Interessierten haben an dieser Stelle die Möglichkeit, ihr Wissen über das jeweilige Thema zu überprüfen. Wenn Sie an den Lösungen des Fragebogens auf der nächsten Seite interessiert sind, schicken Sie uns einfach eine E-Mail mit dem Betreff "Fortbildung im Diabetes-Forum" an heinz@kirchheim-verlag.de . Die richtigen Lösungen schicken wir Ihnen umgehend.
Die Redaktion wünscht Ihnen viel Erfolg!
|
|
Erschienen in: Diabetes-Forum, 2022; 34 (7/8) Seite 28-33