Birkeland et al. analysierten in einer internationalen Beobachtungsstudie mithilfe von Versicherungsdaten die Inzidenz und die Folgen kardiovaskulärer und renaler Endpunkte bei Patienten mit Diabetes mellitus (1 177 896 Patienten) [Birkeland 2020, Birkeland 2021]. Betrachtet wurden Patienten, die initial frei von kardiorenalen Erkrankungen waren (772 336 Patienten). Das mittlere Alter dieser Patienten lag bei 65 Jahren, 45 % waren weiblich, der Beobachtungszeitraum betrug ca. 4,5 Jahre.
Dabei trat bei den bisher gesunden Diabetikern (d. h. ohne initial bekannte kardiovaskuläre oder renale Erkrankung) bei bis zu 11 % der Gruppe neu eine kardiorenale Erkrankung (Herzinsuffizienz oder Nierenerkrankung) auf, was einer Inzidenzrate von ca. 23,5 pro 1 000 Patientenjahren entspricht. Diese kardiorenalen Erkrankungen übertrafen die Inzidenz von Schlaganfall, Myokardinfarkt oder peripherer arterieller Verschlusskrankheit (pAVK) um das bis zu ca. 6-Fache.
- BNP - Brain Natriuretic Peptide
- eGFR - geschätzte glomeruläre Filtrationsrate
- GLP-1 - Glucagon-like Peptide-1
- KDIGO - Kidney Disease: Improving Global Outcomes
- NT-proBNP - N-terminales Fragment des Brain Natriuretic Peptide
- pAVK - periphere arterielle Verschlusskrankheit
- SGLT-2 - Sodium-Glucose Cotransporter 2 (Natrium-Glukose-Cotransporter 2)
Dieses Muster wurde konsistent in allen untersuchten Ländern beobachtet: Das kardiorenale Risiko war deutlich höher als das für Schlaganfall, Herzinfarkt oder pAVK. Weiterhin war das Risiko für die kardiovaskuläre oder Gesamtsterblichkeit bei denjenigen, die ein kardiorenales Syndrom entwickelten, um ca. 3- bzw. 4-fach höher als bei Diabetikern ohne diese Komplikation.
Diese Beobachtungen müssen wir ernst nehmen
Diese Daten müssen uns nachdenklich machen, denn in der Praxis werden häufig Risikofaktoren (wie das HbA1c) erhoben und kontrolliert, eine Screening-Untersuchung für frühe Komplikationen des Diabetes mellitus Typ 2, z. B. Schädigung der Niere oder des Herzens, erfolgt in der Regel jedoch nicht [Shlipak 2021]. Eine weitere Abklärung diesbezüglich erfolgt häufig erst bei Vorliegen von stärkeren Beschwerden und dann wird meist durch Zuweisung zu fachärztlichen Spezialisten (Nephrologen oder Kardiologen) abgeklärt.
Früherkennung gefährdeter Patienten in der hausärztlichen Praxis möglich!
Die Beobachtungen von Birkeland et al. könnten für die Routineversorgung in der Praxis die Konsequenz haben, dass wir zur Früherkennung von kardiovaskulär-renalen Komplikationen eine regelmäßige Testung von Biomarkern durchführen. Unter den möglichen Biomarkern sind
- eGFR (geschätzte glomeruläre Filtrationsrate),
- (Mikro-)Albuminurie und
- NT-proBNP/BNP (N-terminales Fragment des Brain Natriuretic Peptide/Brain Natriuretic Peptide)
dazu besonders geeignet.
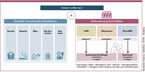
Diese drei genannten Parameter lassen sich niederschwellig im Bereich des Hausarztes bestimmen, ohne dass der Patient einen Extratermin benötigt und zu einem anderen Spezialisten überwiesen werden muss etc. (siehe Abb. 1). Diese Tests ermöglichen im Kontext aller Werte eine individualisierte, risikoadaptierte Beratung und Therapie.
In der Praxis messbare renale Prognoseparameter sind eGFR und Albuminurie
Auch wenn die Beurteilung der Filterfunktion der Niere über die eGFR (berechnet mittels CKD-EPI-Formel) heute fast überall Bestandteil jeder Routine-Laboruntersuchung ist, wird diese meist nur mit dem aktuellen Wert und nicht in deren zeitlichem Verlauf über die Jahre angezeigt. Dadurch wird eine progrediente Verschlechterung der Nierenfunktion mit Rückgang der eGFR nur schwer erkannt. In der Praxis hat sich außerdem etabliert, eine eGFR bis 60 ml/min als normal zu akzeptieren, weil viele Medikamente erst ab dieser eGFR in der Dosis reduziert werden müssen oder sogar kontraindiziert sind. Diese Simplifizierung entspricht aber nicht mehr den neuen Empfehlungen der Organisation KDIGO (Kidney Disease: Improving Global Outcomes) [Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group 2020], nach denen bei einer eGFR zwischen 60 und 89 ml/min (Stadium G2) bereits eine milde Nierenschädigung vorliegt.
Der zweite wesentliche Nierenparameter, die Albuminurie (früher Mikroalbuminurie), wird häufig in der Praxis nicht routinemäßig bestimmt, wodurch prognose- und therapierelevante Informationen verloren gehen. Denn bei Vorliegen einer Albuminurie muss auch von einer generellen vaskulären Schädigung ausgegangen werden: Wie seit Langem bekannt ist, ist das kardiovaskuläre Risiko dieser Patienten deutlich erhöht [Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group 2020, Weir 2007].
Sowohl eGFR als auch Albuminurie sind daher wesentliche, komplementäre Bestandteile zur Beurteilung der Nierenfunktion und -schädigung. Sie stellen den modernen Standard der Beurteilung der Nierenfunktion – aber auch des kardiovaskulären Risikos – dar [Kidney Disease: Improving Global Outcomes (KDIGO) Diabetes Work Group 2020, Weir 2007].
Natriuretische Peptide – neue Marker zum Herzinsuffizienz-Screening in der Praxis?
Typ-2-Diabetiker weisen häufig frühe und auch asymptomatische Formen der Herzinsuffizienz (z. B. Relaxationsstörungen, diastolische Dysfunktionen) auf. Das erhöht das Risiko der Entwicklung einer klinischen Herzinsuffizienz deutlich. Diese frühen Formen der Herzdysfunktion entgehen bis heute der Diagnose in der Regelversorgung. Erst wenn Diabetiker z. B. mit Luftnot symptomatisch werden, werden weitere Untersuchungen – z. B. Echokardiographie – in Betracht gezogen.
Eine in der Praxis einfach durchzuführende Methode zur Analyse von kardialen Dysfunktionen ist die Bestimmung von natriuretischen Peptiden, die seit Jahren etabliert ist und in den Leitlinien empfohlen wird [Sweeney 2019].
Risikoerkennung in der Praxis – müssen wir umdenken?
Es ist daher zu überlegen, ob neben der regelmäßigen Kontrolle der Risikofaktoren zumindest einmal im Jahr eine Risikoerfassung stattfinden sollte (siehe Abb. 1), bei der genau diese drei Parameter eGFR, Albuminurie und natriuretische Peptide gemessen werden sollten. Sind diese Untersuchungen alle negativ bzw. unauffällig, kann zunächst von einem niedrigen kardiorenalen Risiko ausgegangen werden.
Bei Auffälligkeiten sollte frühzeitig und vorrangig die Zuweisung zum Spezialisten erfolgen. Denn bei diesen Patienten besteht Handlungsbedarf aufgrund des erhöhten kardiorenalen Risikos, wie Birkeland et al. gezeigt haben.
Früherkennung ermöglicht früheres Handeln
Bei auffälligen Biomarkern (siehe Abb. 1) sollte der Patient zügig und mit Priorität zu den entsprechenden Spezialisten geschickt werden, z. B. für Echokardiographie, Belastungs-Untersuchungen, Koronarangiographie oder aber auch zur weiteren nephrologischen Abklärung. Parallel dazu sollte eine konsequente und evidenzbasierte Therapie der bekannten kardiovaskulären Risikofaktoren wie Hypertonie, Dyslipidämie und Hyperglykämie erfolgen [Buse 2020, Cosentino 2020, Davies 2018].
Fazit für die Praxis
Die positiven Studiendaten für die SGLT-2-Hemmer und GLP-1-Rezeptoragonisten zur Reduktion kardiovaskulärer Ereignisse und der Verbesserung der renalen Parameter haben zu einem Paradigmenwechsel geführt:
Ausblick
Die neuesten Daten zur Verbesserung der Prognose bei Patienten mit Herzinsuffizienz (DAPA-HF, EMPEROR-Reduced, SOLOIST-WHF) und auch Patienten mit chronischer Nierenerkrankung (DAPA-CKD und SCORED) unterstreichen die Vorteile der SGLT-2-Hemmer gerade in diesen kardiorenalen Risikogruppen (DAPA-HF: Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure, EMPEROR-Reduced: EMPagliflozin outcomE tRial in Patients With chrOnic heaRt Failure With Reduced Ejection Fraction, SOLOIST-WHF: Effect of Sotagliflozin on Cardiovascular Events in Patients With Type 2 Diabetes Post Worsening Heart Failure, DAPA-CKD: A Study to Evaluate the Effect of Dapagliflozin on Renal Outcomes and Cardiovascular Mortality in Patients With Chronic Kidney Disease, SCORED: SCreening for Occult REnal Disease).
Danksagung: Dieser Kommentar wurde erstellt mit der freundlichen Unterstützung von AstraZeneca.
Erschienen in: Diabetes, Stoffwechsel und Herz, 2021; 30 (1) Seite 22-24