Die Thromboseprophylaxe ist – wie die aktuelle Corona-Pandemie zeigt – besonders bei Menschen mit Diabetes und/oder Adipositas extrem wichtig. Die Anfänge dazu reichen zurück bis in das Jahr 1884, als man die Substanz Hirudin im Kopf von Blutegeln nachweisen und schließlich zur Thrombose-Verhinderung als Medikament einsetzen konnte.
Seit 1915 gibt es die Heparine zur subkutanen Injektion, seit 1922 die Kumarine, einen Vorläufer des Marcumar®.
Vitamin-K-abhängige Gerinnungshemmer
- Marcumar®
- Falithrom®
- Coumadin®
Die neueren gerinnungshemmenden Medikamente konnten erst, wie schon erwähnt, entwickelt werden, nachdem 1915 durch Morawitz das Grundschema der Blutgerinnung beschrieben wurde. Die allerneuesten Gerinnungshemmer wie z.B. die direkten Faktor Xa-Hemmer, sowie die direkten Thrombinhemmer stellen die aktuell am Weitesten entwickelte Möglichkeit der Blutgerinnungshemmung dar.
Studien Jahre zuvor hatten gezeigt, dass ein Molekül Faktor Xa in der Lage ist, 1000 Thrombin-Moleküle zu generieren. Durch die Hemmung von Faktor Xa ist daher die Thrombinbildung schon in einem sehr frühen Stadium sehr gut zu unterbinden.
Bisher wurden Patienten im Krankenhaus meist mit niedermolekularen Heparinen o.ä. s.c. behandelt und später auf Tabletten umgestellt. In vielen Fällen erfolgt heute direkt oder einige Stunden nach z.B. einer Operation bereits eine Umstellung auf die neueren Nicht-Vitamin-K-abhängigen Gerinnungshemmer (NOAK).
Eine Hemmung der Blutgerinnung wird schon Jahrzehnte durch die Hemmung der in der Leber gebildeten Blutgerinnungsfaktoren z.B. II, VII, IX und X, die Vitamin-K-abhängig sind (z.B. durch Marcumar®!), durchgeführt. Die nicht Vitamin-K-abhängigen Blutgerinnungshemmer (NOAK) hemmen dagegen entweder gezielt den Faktor Xa (Rivaroxaban, Apixaban und Edoxaban) oder das für die Blutgerinnung ebenfalls erforderliche Thrombin (Faktor II- Hemmer/Dabigatran) direkt – also gezielt jeweils nur einen Gerinnungsfaktor.
Neue Antithrombotika (Tabletten)
- Pradaxa® (Dabigatran) – direkter Thrombinhemmer (=Faktor II-Hemmer)
- Xarelto® (Rivaroxaban) – direkter Faktor Xa-Hemmer
- Eliquis® (Apixaban) – direkter Faktor Xa-Hemmer
- Lixiana® (Edoxaban) – direkter Faktor Xa-Hemmer
Antidots gibt es für alle Gerinnungshemmer
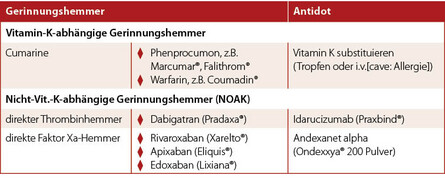
Als Antidot z.B. bei einer Blutung unter einer Marcumar-Therapie gilt das Vitamin K. Von den neueren Nicht-Vit.-K-abhängigen Blutgerinnungshemmern gibt es mittlerweile sowohl ein Antidot gegen den direkten Thrombinhemmer Dabigatran (= Idarucizumab/Praxbind®) als neuerdings auch gegen die Faktor Xa-Hemmer Rivaroxaban (Xarelto®) und Apixaban (Eliquis®) (Andexanet alpha, Ondexxya®200 Pulver). Diese Substanzen sind in großen Kliniken mit Intensivstation in der Regel vorhanden – sie werden aber wegen möglicher Nebenwirkungen (z.B. überschießender Gegenregulation) nur gezielt eingesetzt. Eine Blutung unter diesen Substanzen wird in der Regel primär durch die Gabe von Blutkonserven und auch "Frischplasma" (PPSB) behandelt.
Ein Vorteil der NOAK - Blutgerinnungshemmer (=Nicht-Vitamin-K-Abhängige oralen Antikoagulantien) ist, dass sie weitgehend unabhängig vom Gewicht eines Patienten sind. Es ist unerheblich ob der Patient 60kg oder 140kg wiegt, die Dosis ist dieselbe. Eine Anpassung der Dosierung erfolgt lediglich z.B. bei Niereninsuffizienz/schwerer Lebererkrankung. Ein weiterer Vorteil ist, dass keine speziellen Tests wie bei der Marcumar®-Therapie (INR, Quick= Thromboplastinzeit) zur Steuerung der Therapie durchgeführt werden müssen. Nach wie vor aber ist nach Implantation z.B. einer mechanischen Herzklappe nur eine Dauertherapie mit Vitamin-K-Antagonisten z.B. mit Cumarinen, wie Marcumar® zugelassen – die neueren nicht Vitamin-K-abhängigen Antikoagulantien sind sogar kontraindiziert.
Behandlungsstrategie bei Hämophilie A und B
85% der Hämophilie-Patienten haben eine Hämophile A (Faktor VIII-Mangel), 15% eine Hämophilie B (Faktor IX-Mangel = Christmas-Faktor). Die Hämophilie A wird in 70% X-chromosomal -rezessiv vererbt, 30% sind sporadisch, d.h.es handelt sich um Spontanmutationen des X-Chromosoms. Es sind meist nur Männer betroffen.
- Alle Töchter eines Bluters sind Konduktorinnen, sie haben vom Vater das kranke X-Chromosom.
- Alle Söhne eines Bluters mit einer genetisch gesunden Frau sind gesund – sie haben das gesunde Gen der Mutter.
Je nach Restaktivität von Faktor VIII bezeichnet man eine Hämophilie als:
- Leicht, etwa 4-40% Restaktivität
- Moderat, etwa 1-5% Restaktivität
- Schwer, bei weniger als 1% Restaktivität
Die Behandlung und Betreuung von Hämophilie-Patienten erfolgt in entsprechenden Zentren!
Empfehlungen sind:
- Prophylaktisch: Meiden von Gelenkverletzungen
- Meiden von Nicht-steroidalen Antirheumatika
- Blutstillung lokal mit z.B. Fibrinklebern, Antifibrinolytika
- Gabe von Gerinnungsfaktoren nach den Leitlinien der World Federation of Haemophilia = WFH
Therapie bei Thrombosen
Medikamentöse Therapie: Lyse-Therapie
Die medikamentöse Behandlung mit Aktivatoren der Fibrinolyse erfolgt z.B. bei:
- Schwerer Lungenembolie
- Frischem Herzinfarkt
- Phlegmasia coeulea dolens
- Frische, proximale Thrombosen im Becken-Oberschenkel-Bereich
Dies erfolgt mit:
- Alteplase (rtPA= Actilyse®)
- Reteplase (rPA)
- Tenecteplase
- Selten noch Urokinase
Danach weitere Antikoagulation nach den Leitlinien der Fachgesellschaften
Nicht-medikamentöse Therapie
Als nicht-medikamentöse Therapie kommt die Thrombektomie in Frage oder eine Katheter-Thrombolyse- und Thrombektomie. (n. Herold, 2023)
Therapie des Antiphospholipid-Syndroms
Es zeichnet sich aus durch hohe Titer an Antiphospholipid-Antikörpern mit den Symptomen:
- Arterielle und/oder venöse Thrombosen
- Häufigen (Früh-)Aborten
- Thrombozytopenien
In diesen Fällen erfolgt eine Langzeittherapie mit Phenprocoumon evtl. auch niedermolekularen Heparinen, evtl. Acetylsalicylsäure
Therapie der Verbrauchskoagulopathie
Ausgelöst durch verschiedene Erkrankungen kann es zu einer generalisierten Bildung von kleinen Mikrothromben in der Endstrombahn des Blutgefäßsystems eines Menschen kommen. Dadurch kommt es zu einem Verbrauch (= Abfall der Thrombozyten!) von Zellen und Gerinnungsfaktoren – später zu einer sekundären Hyperfibrinolyse (= Gerinnsel werden wieder z.T. überschießend aufgelöst (=Blutung). Dies kann in ein Multiorganversagen münden, z.B. bei bakterieller Sepsis, aber auch im Rahmen von Operationen an bestimmten Organen (4 "P"), z.B. an der Lunge (Pulmo), Pankreas, Prostata, Plazenta (n. Herold 2024).
Die Therapie erfolgt nach kausalen und symptombezogenen Gesichtspunkten. Dabei darf Heparin nur unter Vorbehalt gegeben werden.
Medikamente zur Hemmung des fibrinolytischen Systems
Im Körper selbst sind physiologischerweise Alpha-2-Antiplasmin und Plasminogen-Aktivator-Inhibitor (PAI) aktiv.
Therapeutisch medikamentös ist es z.B. die Tranexansäure. Diese wird gegeben z.B. als Antidot
- bei Blutungen unter der Therapie mit Fibrinolytika
- Blutungen bei Polytrauma,
- Peripartal etc.,
- Nasenbluten bei M. Osler
|
|
Erschienen in: Diabetes-Forum, 2024; 36 (4) Seite 16-18


